
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Расчет рН в растворах слабых кислот и оснований
Диссоциация многих электролитов протекает не полностью. Отношение числа диссоциированных молей к общему числу молей электролита в растворе называют степенью диссоциации. Для его количественного описания используют константу равновесия, называемую константой диссоциации. Для одноосновной кислоты, диссоциирующей по уравнению:
| НАn Û Н+ + Аn-, где Аn - кислотный остаток, | |
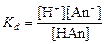 . .
| (62) |
Т.к. [An–] = [H+] и [An] = C то 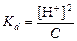 и
и
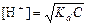 , ,
| (63) |
где С – концентрация слабой кислоты, моль/л Kd – константа диссоциации (приводится в справочниках).
Для растворов слабых оснований:
 , ,
| (64) |
где С - концентрация слабого основания, моль/л.
По значению константы диссоциации можно рассчитать степень диссоциации слабого электролита:
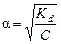 . .
| (65) |
Многоосновные кислоты диссоциируют ступенчато, например: Н2S Û НS- + Н + (1-ая ступень); НS- Û S2- + Н+ (2-ая ступень).
При расчетах рН обычно учитывают только первую ступень диссоциации, пренебрегая второй и третьей ступенями. Таким образом, уравнения (62 и 64) справедливы и для многоосновных кислот при использовании первой константы диссоциации Kd 1.
Date: 2015-09-24; view: 761; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |