
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Катализ - - это изменение скорости химических реакций под воздействием вешеств, количество и природа которых после завершения реакции остаются такими же, как и до реакции
Катализатор — нерасходуемый реагент, увеличивающий скорость реакции. В отличие от катализаторов ингибиторы -вещества, препятствующие протеканию реакции, они расходуются в ходе реакции. Катализ бывает гомогенным и гетерогенным. При гомогенном катализе катализатор вместе с реагентами образует раствор. Гетерогенный катализ происходит на поверхности твердого катализатора, а реагирующие вещества входят в состав газовой смеси или жидкого раствора.
Любые каталитические реакции обладают общими для них особенностями.
Катализатор не оказывает влияния на глубину протекания
реакции, т. е. на ее равновесие и константу равновесия (см. гл. 4).
Он лишь ускоряет реакцию.
Катализаторы по своему действию селективны, т. е. избирательны. Они ускоряют только одну или две-три из большого числа возможных реакций. Например, из этилового спирта можно получить следующие продукты: уксусный альдегид, этилуксусный эфир, бутадиен, ацетон, ацетилен, но каждая из реакций превращения этилового спирта проходит только в присутствии «своего» специфического катализатора.
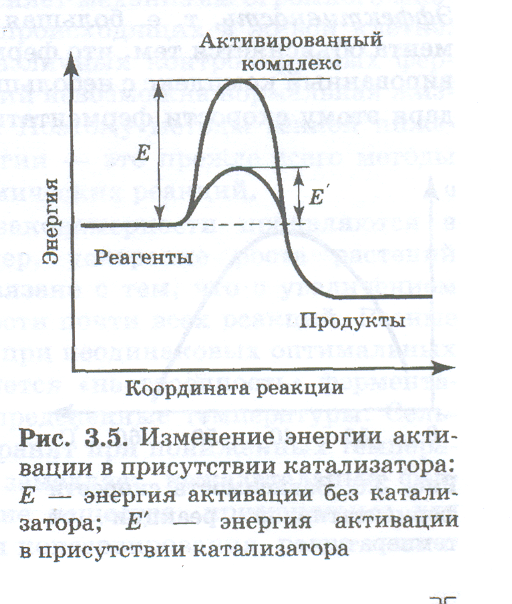
Ускоряющая роль катализатора объясняется тем, что ктивированный комплекс, образованный с участием катализатора, имеет более низкую энергию активации, чем активированный комплекс, возникающий в отсутствие катализатора (рис. 3.5). Скорость реакции в присутствии катализатора пропорциональна концентрации (гомогенный катализ) или поверхности (гетерогенный катализ) катализатора.
Почти все биохимические реакции в клетках животных и растений проходят с участием ферментов.
Ферменты — белки, которые катализируют химические реакции в биологических системах.
Другое название ферментов — энзимы. В природе известны десятки тысяч ферментов. Строение многих из них сходно для растительных и животных клеток, для высших и простейших организмов. От прочих катализаторов они отличаются весьма сложным молекулярным строением, эффективностью, специфичностью и чувствительностью к внешним условиям.
Молекула фермента обычно представляет собой клубок из больших белковых цепей — глобулу. На поверхности глобулы или в особом углублении располагается сравнительно небольшой по размерам участок — активный центр, который выполняет две функции: распознавание и катализ. Распознавание субстрата — вещества, на которое способен воздействовать данный фермент, — осуществляется за счет точного соответствия между формами и размерами молекулы субстрата и активного центра, как у ключа в замке. Благодаря такому соответствию многие ферменты проявляют высокую специфичность — способность катализировать превращение только одного вещества. Подошедшая из раствора к глобуле фермента молекула субстрата связывается и ориентируется ферментом таким образом, чтобы активный центр мог осуществлять превращение субстрата. Эффективность* т. е. большая ускоряющая способность фермента объясняется тем, что фермент и субстрат образуют активированный комплекс с небольшой энергией активации. Благодаря этому скорости ферментативных реакций в 109—1012 раз выше, чем у обычных, неферментативных превращений. Часто для осуществления каталитического действия активного центра бывают необходимы коферменты — небольшие небелковые молекулы или катионы металлов калия, магния, марганца, меди, железа и никеля Коферменты входят в состав образующегося в активном центре активированного комплекса с субстратом.
Действие ферментов в существенной степени зависит от состава раствора, в том числе от кислотности среды. Для каждого фермента существует оптимальная температура, при которой он в наибольшей степени проявляет свою каталитическую активность (рис. 3.6). Вплоть до
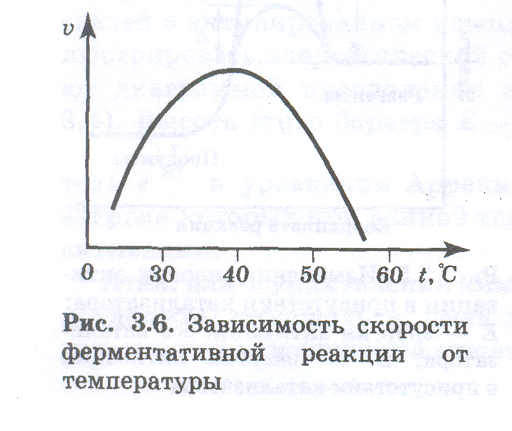
достижения этой температуры скорости ферментативных реакций возрастают в соответствии с уравнением Аррениуса. Причем числовое значение температурного коэффициента γ для таких реакций может быть значительно большим, чем предсказываемое правилом Вант-Гоффа. Для большинства ферментов оптимальная температура находится в пределах от 40 до 50 °С. При более высоких температурах ферменты теряют свою активность, вследствие тепловой денатурации их белковая часть свертывается подобно тому, как свертывается при варке белок куриного яйца.
Date: 2015-09-18; view: 534; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |