
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Реакции окисления
1. Бензольное кольцо в обычных условиях с трудом окисляется в присутствии пятиокиси ванадия V2O5:
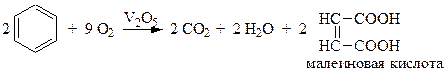
2. Окисление алкилпроизводных бензола идет с образованием карбоксилсодержащих бензольных производных:



3. Озонолиз:

4. Каталитическое окисление О2 в присутствии медного катализатора.

Правила ориентации в бензольном ядре
Наличие заместителя в молекуле бензола требует ответа на два вопроса:
1. Какое влияние оказывает заместитель на скорость реакции – замедляет или ускоряет ее по сравнению со скоростью реакции незамещенного бензола?
2. В какое положение бензольного кольца он направляет электрофильную частицу Е+?
Эти вопросы связаны с перераспределением электронной плотности в бензольном кольце.
Рассмотрим два типа заместителей:

Метильная группа проявляет донорные свойства по отношению к бензольному кольцу за счет +I эффекта и эффекта гиперконъюгации (сверхсопряжения), что приводит к повышению электронной плотности в о - и п- положениях и, следовательно, к активации молекулы толуола в реакциях с электрофильными агентами и вступлению нового заместителя именно в о - и п- положения. Нитрогруппа обладает электроноакцепторными свойствами по отношению к бензольному кольцу из-за сильных –М и –I эффектов. Это приводит к уменьшению электронной плотности в о - и п- положениях бензольного кольца и дезактивации нитробензола по сравнению с незамещенным бензолом. м -Положения молекулы нитробензола менее чувствительны к влиянию нитрогруппы, частичный положительный заряд на этих атомах углерода меньше, чем в о - и п- положениях, поэтому в этом случае атака электрофила происходит в м -положение бензольного кольца.
Таким образом, электронодонорные заместители увеличивают электронную плотность в бензольном кольце и облегчают атаку электрофилом, замещение происходит в о - и п- положения. Реакции проходят быстрее, чем в случае незамещенного бензола. Электронодонорными свойствами обладают следующие заместители:
-NH2, -NHR, -NR2, -OH, -OR, -R (алкил)
Ряд по увеличению активности электронодонорных заместителей (увеличение скорости реакции):
NH2 > OH > OR > Cl > I > CH3
Электроноакцепторные заместители, напротив, понижают электронную плотность в бензольном кольце, что затрудняет взаимодействие с электрофилом и приводит к снижению скорости реакции замещения по сравнению незамещенным бензолом, атака электрофилом осуществляется в м -положения бензольного кольца. Акцепторными свойствами обладают следующие функциональные группы:

Ряд по увеличению активности электроноакцепторных заместителей (уменьшение скорости реакции):

Особенности влияния галогенов. Галогены дезактивируют молекулу бензола в реакциях электрофильного замещения, но направляют электрофильный агент в о - и п -положения бензольного кольца. Это связано с тем, что –I – эффект атомов галогенов сравним с +М – эффектом.

Таблица 10.1
Date: 2016-02-19; view: 487; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |