
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Правила заполнения энергетических уровней
Распределение электронов по уровням происходит по общему правилу: электроны невозбужденного атома занимают состояния с наименьшей энергией и в соответствии с принципом Паули, который гласит: в атоме не может быть даже двух электронов с одинаковым набором квантовых чисел.
Совокупность электронов с одним и тем же n образуют слой. В каждом слое электроны с данным значением l образуют оболочку. (Примечание: иногда в литературе слой называют «оболочкой», в этом случае электроны с одним l образуют «подоболочку»).
| главное квант. число - n | |||||||||||
| символ слоя | K | L | M | N | O | ||||||
| макс. число электронов в слое | |||||||||||
| орбитальное квант. число – l | |||||||||||
| символ оболочки | 1s | 2s | 2p | 3s | 3p | 3d | 4s | 4p | 4d | 4f | |
| макс. число электронов в оболочке |
Заполнение по этому признаку идет до 18Ar (аргон). У следующих за ним атомов 19К и 20Са, заполняются оболочки 4s. Это связанно с тем, что из-за более сильного экранирования электронов оболочки 3d, оболочка 4s характеризуется более низкой энергией.
В целом заполнение слоев происходит по правилам Клечковского:
1. От оболочек с меньшим значением суммы квантовых чисел (n+l) к оболочкам с большей суммой (n+l).
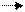
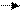 Пример: 18Ar 3p (3+1) = 4
Пример: 18Ar 3p (3+1) = 4
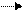
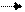 19К 3d (3+2) = 5
19К 3d (3+2) = 5

 19К 4s (4+0) = 4 – реализуется.
19К 4s (4+0) = 4 – реализуется.
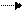
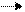 20Са 4s (4+0) = 4, s – оболочка заполнена.
20Са 4s (4+0) = 4, s – оболочка заполнена.

 21Sc 3d (3+2) = 5
21Sc 3d (3+2) = 5
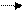 4p (4+1) = 5 Какая из них реализуется?
4p (4+1) = 5 Какая из них реализуется?
2. При одинаковом значении (n+l) – от оболочек с меньшим n к оболочкам с большим n.
Это значит в 21Sc (Sc - скандий) будет заполняться 3d оболочка.
У этих правил, есть исключения, например, лантан – 57La, церий – 58Cc и элементы 7–ой группы таблицы Менделеева.
Анализ хода заполнения оболочек у разных химических элементов показывает:
1. Общее число электронов в атоме химического элемента, а следовательно и заряд ядра, равно порядковому номеру элемента в периодической таблице Менделеева.
2. Число электронных слоев равно номеру периода, к которому относится элемент.
3. Число электронов во внешнем слое равно номеру группы, занимаемой элементом в этой таблице.
Date: 2015-05-19; view: 710; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |