
Полезное:
Как сделать разговор полезным и приятным
Как сделать объемную звезду своими руками
Как сделать то, что делать не хочется?
Как сделать погремушку
Как сделать так чтобы женщины сами знакомились с вами
Как сделать идею коммерческой
Как сделать хорошую растяжку ног?
Как сделать наш разум здоровым?
Как сделать, чтобы люди обманывали меньше
Вопрос 4. Как сделать так, чтобы вас уважали и ценили?
Как сделать лучше себе и другим людям
Как сделать свидание интересным?

Категории:
АрхитектураАстрономияБиологияГеографияГеологияИнформатикаИскусствоИсторияКулинарияКультураМаркетингМатематикаМедицинаМенеджментОхрана трудаПравоПроизводствоПсихологияРелигияСоциологияСпортТехникаФизикаФилософияХимияЭкологияЭкономикаЭлектроника

Изучение реакции комплексообразования с органическим лигандом
Сульфосалициловая кислота образует с ионами Fe3+ окрашенные комплексные соединения разного состава и цвета в зависимости от рН раствора. При рН 1,8 – 2,5 образуется красно-фиолетовый катионный комплекс, имеющий полосу поглощения с λmax = 510 нм (I).
При увеличении рН до 4 – 8 раствор приобретает красно-бурую окраску, которую приписывают анионному бис-комплексу (II):
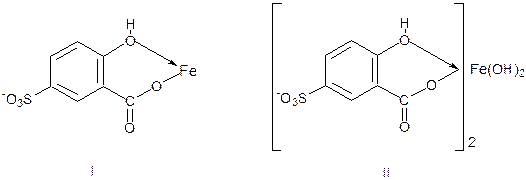
В щелочных средах (9<рН<11,5) образуется комплекс желтого цвета с полосой поглощения λmax = 416 нм. При рН>12 происходит его разложение с выпадением в осадок гидроксида железа. Ранее предполагалось, что образующийся в щелочных средах комплекс является трисульфосалицилатом железа(III). Однако в настоящее время его образование связывают не с присоединением третьей молекулы реагента, а с депротонированием бис-комплекса:
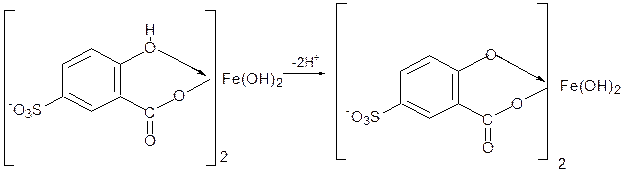
Депротонированный желтый комплекс железа(III) достаточно устойчив и позволяет проводить определение железа в присутствии ацетат-, борат-, фосфат- и фторид-ионов. Ионы Al(III), Sn(II) и некоторые другие образуют бесцветные комплексы, не мешающие определению железа(III). В этом случае прибавляют избыток реактива. Медь(II) образует менее устойчивый сульфосалицилатный комплекс и обнаружению железа(III) в кислой среде не мешает.
Обнаружение Fе3+ в виде сульфосалицилатного комплекса
К 3-5 каплям анализируемого раствора прибавляют 3-5 капель раствора сульфосалициловой кислоты; Появление буро-фиолетовой окраски (если рН=2) указывает на присутствие Fe3+ в растворе. Если окраски нет, то наличие Fe3+ в растворе не исключено, так как рН раствора может быть меньше 1 (что не фиксируется универсальным индикатором), в растворе могут быть бесцветные комплексы железа(III). К раствору прибавляют по каплям раствор концентрированного NH4OH до рН = 10. Появление желтой окраски указывает на присутствие железа(III). Параллельно ставят контрольный опыт.
Date: 2015-05-17; view: 1981; Нарушение авторских прав; Помощь в написании работы --> СЮДА... |